Anvisa registra primeiro teste de farmácia para detecção do HIV
Ideia do registro do autoteste do vírus da aids vinha sendo estudada desde 2015, ano em que a Anvisa havia regulado o registro de produtos para diagnóstico in vitro do HIV
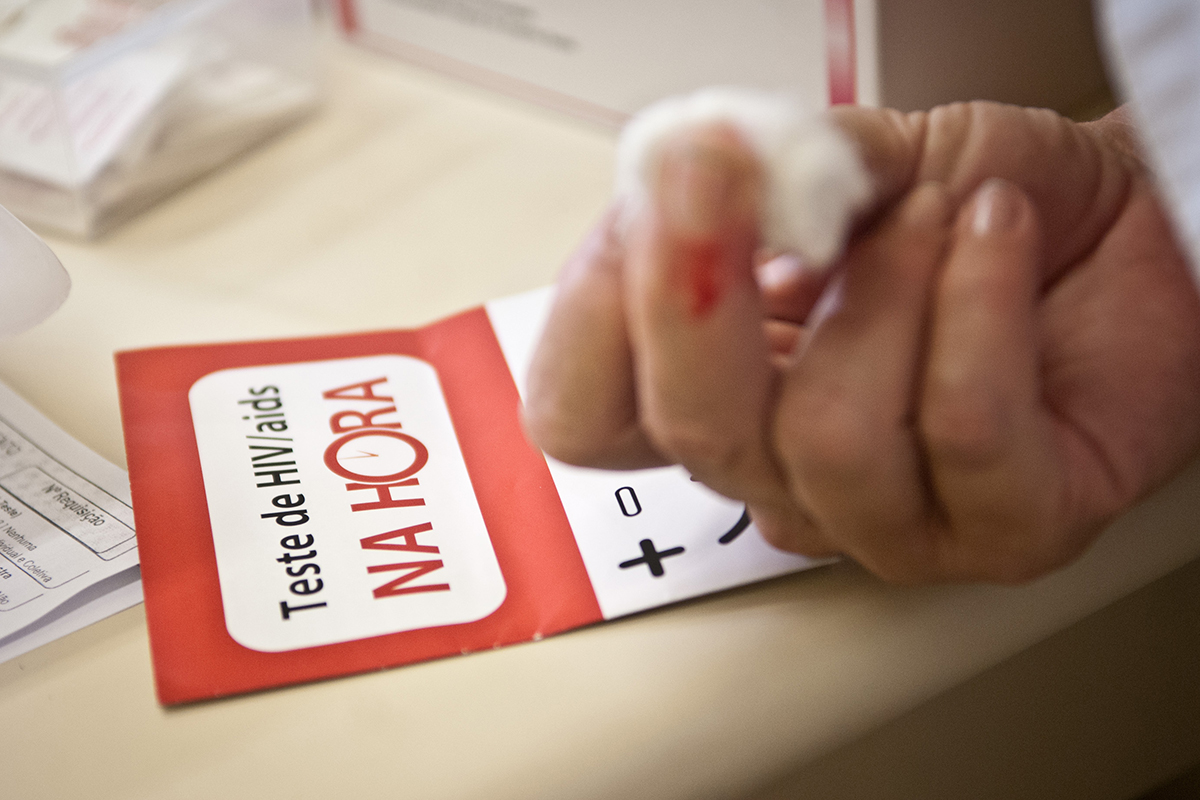
A Agência Nacional de Vigilância Sanitária (Anvisa) registrou esta semana o primeiro autoteste para detectar o HIV a ser comercializado em farmácia, como outros testes comuns. O Action, nome comercial do produto, será fabricado pela empresa Orangelife Comércio e Indústria e dará o resultado em até 20 minutos. O valor do teste será definido pelo fabricante.
A ideia do registro do autoteste do vírus da aids vinha sendo estudada desde 2015, ano em que a Anvisa havia regulado o registro de produtos para diagnóstico in vitro do HIV.
Assim como alguns aparelhos que são usados para a medição de glicose por diabéticos, o teste de HIV vem com um líquido reagente, uma lanceta específica para furar o dedo, um sachê de álcool e um capilar (tubinho para coletar o sangue). O resultado aparece na forma de linhas que indicam se há ou não presença do anticorpo do HIV. A presença do anticorpo mostra que a pessoa foi exposta ao vírus que provoca a aids.
Apesar de demonstrar 99,9% de sensibilidade e efetividade, o teste só poderá indicar a presença do vírus 30 dias depois da situação de exposição. Caso o teste dê positivo, a pessoa deve procurar um serviço de saúde. Em caso de resultado negativo, o teste deverá ser repetido após 30 dias.
A situação de exposição começa a contar a partir do momento em que a pessoa possa ter tido o contato com o vírus da aids, seja em uma relação sexual sem proteção ou com o compartilhamento de agulhas. O tempo de 30 dias é o período que organismo precisa para produzir anticorpos em níveis que o autoteste consegue detectar.
Se uma nova situação de exposição ocorrer após este período um novo teste precisa ser feito, respeitando o prazo necessário para detecção e as confirmações necessárias.


